Sie sind hier: Startseite > Prostata > Operationen > Prostatabiopsie
Transrektale und Perineale Prostatabiopsie: Technik und Komplikationen
Indikation zur Prostatastanzbiopsie
Die Prostatabiopsie ist indiziert bei Verdacht auf Prostatakarzinom, wie bei suspekter rektaler Untersuchung, erhöhtem PSA-Wert oder suspekter Bildgebung im Multiparameter-MRT der Prostata. Siehe Kapitel Prostatakarzinom.
Kontraindikationen
Harnwegsinfektion, Prostatitis, fehlendes Rektum, Kontraindikationen für Steinschnittlage. Gerinnungsstörungen und andere Krankheiten, die gegen einen elektiven planbaren Eingriff sprechen.
Technik der Prostatastanzbiopsie
Patientenvorbereitung:
Ausschluss oder Therapie einer Harnwegsinfektion. Die Keimlast im Rektum sollte vor der transrektalen Biopsie mit Povidon-Iod Zäpfchen reduziert werden.
Perioperative Antibiotikaprophylaxe: Standardempfehlung war lange Zeit ein lang wirkendes Fluorchinolon oral über 1–3 Tage: zum Beispiel Ciprofloxacin 500 mg 1–0–1. Aufgrund potentiell schwerwiegender Nebenwirkungen haben Fluorchinolone die Zulassung für die prophylaktische Anwendung verloren (Arzneimittelkommission, 2019). Alternative Antibiotika sind: Aminopenicilline, Gentamicin oder Cephalosporine, die teilweise in Kombination eingesetzt werden. Ein aktueller Standard existiert nicht. Fosfomycin wurde 2022 in Deutschland die Zulassung zur Antibiotikaprophylaxe bei Prostatabiopsie entzogen. Bei der perinealen Stanzbiopsie ist eine Antibiotikaprophylaxe nicht zwingend erforderlich.
Anästhesie der Prostatabiopsie:
Periprostatische Infiltrationsanästhesie mit einem Lokalanästhetikum, am besten in Kombination mit einem Diclofenac-Suppositorium. Dazu werden vor der Biopsie 20 ml Lokalanästhetikum im Bereich der neurovaskulären Bündel beidseits der Prostata infiltriert. Bei der transperinealen Biopsie werden zusätzlich die Haut und der Nadelweg durch den Beckenboden infiltriert. Für Stanzbiopsien mit einer hohen Stanzzylinderanzahl ist eine Spinal- oder Allgemeinanästhesie sinnvoll.
Punktionstechnik bei der Prostatabiopsie:
Es wird eine transrektale oder transperineale Stanzbiopsie mit einer 18G-TrueCut Stanznadel mit Stanzpistole unter transrektaler Ultraschallkontrolle durchgeführt.
Anzahl und Lokalisation der Stanzzylinder:
Das Minimum sind sechs Stanzzylinder (Sextantenbiopsie), drei aus jedem Prostataseitenlappen (apikal, Mitte und basal) [Sextantenbiopsie] (Hodge u.a., 1989). Die EAU-Leitlinie zum Prostatakarzinom empfiehlt mindestens 10 Stanzzylinder [Heidenreich (Eur Urol 2008)]. Suspekte (hypoechogene) Läsionen der Prostata sollten zusätzlich biopsiert werden, da hier eine erhöhte Wahrscheinlichkeit für ein Prostatakarzinom besteht. Die Stanzzylinder werden in getrennten Kassetten zum Pathologen geschickt, um später Rückschlüsse auf die Tumorlokalisation zu ermöglichen (vor Nerverhaltung bei der radikalen Prostatektomie).
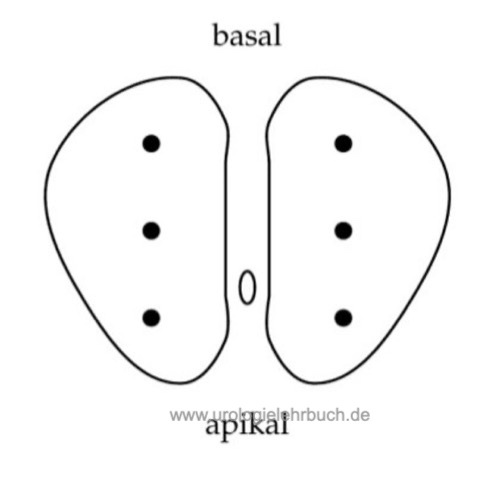 |
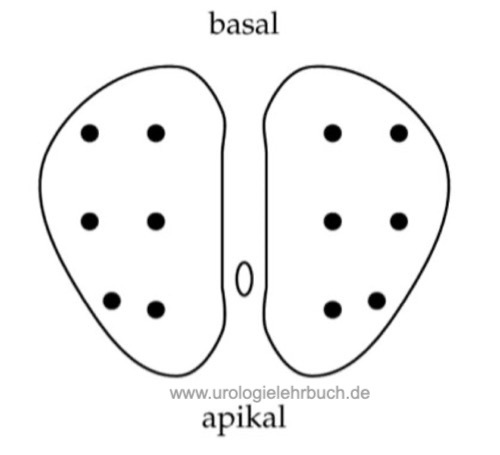
Eine kapselnahe Sextantenbiopsie detektiert mehr Karzinome (Stamey, 1995). Da die Stanzpistole die Nadel um 2 cm in das Gewebe hineinbewegt, muss diese Strecke vor der Biopsie eingeplant werden. Besonders bei apikalen Stanzbiopsien kann der dorsale Venenplexus verletzt werden. In prospektiven Studien konnte durch die Erhöhung der Stanzzylinderzahl eine verbesserte Sensitivität nachgewiesen werden. Die zusätzlichen Stanzen sollten lateral nahe der Organkapsel und aus der Übergangszone entnommen werden [Abb. 1.2]. Eine Erhöhung der Stanzzylinderzahl erhöht jedoch auch das Risiko, ein nicht signifikantes Prostatakarzinom zu diagnostizieren. 80 % der Karzinome werden mit der ersten Stanze diagnostiziert, 10 % mit der zweiten, 7 % mit der dritten und 3 % mit der 4. Stanze.
 |
MRT-(Fusions)biopsie:
Voraussetzung ist ein Multiparameter-MRT (mpMRT) zur Lokalisation eines möglichen Prostatakarzinoms, mit verschiedenen Techniken kann eine gezielte Biopsie der suspekten Areale durchgeführt werden. In wenigen prospektiven Studien konnten keine klinisch relevanten Unterschiede zwischen Hardware-unterstützter und kognitiver Fusion festgestellt werden (Lee u.a., 2016) (Puech u.a., 2013) (Wegelin u.a., 2019) (Wysock u.a., 2014).
MRT-Biopsie:
Die in-bore MRT-Biopsie wird während der MRT-Untersuchung durchgeführt. Die Technik ist sehr aufwendig und wird selten angewandt.
Fusionsbiopsie:
Die Bilddaten des mpMRT werden anhand von Bezugspunkten mit dem Ultraschallbild fusioniert, um gezielt Stanzbiopsien zu entnehmen. Das Gerät kann die Bewegung des Ultraschallkopfes mit den fusionierten Bilddaten verknüpfen, so dass die Region of Interest (ROI) während der Sonographie angezeigt wird. Die Soft- und Hardware für die Fusionsbiopsie sind noch sehr teuer.
Kognitive Fusion:
Kostengünstigste Methode, die eine gute räumliche Orientierung in der Prostata mittels transrektaler Sonographie voraussetzt. Die suspekten Areale der MRT-Untersuchung werden "in Gedanken" mit dem Bild der transrektalen Sonographie verknüpft und so eine "gezielte" Biopsie durchgeführt.
Komplikationen der Prostatastanzbiopsie
Geringgradige Komplikationen sind mit über 50 % relativ häufig, schwerwiegende Komplikationen sehr selten (Rodriguez und Terris, 1998).
Infektionen:
Harnwegsinfektionen, bakterielle Prostatitis, selten Urosepsis (1 % bei transrektaler Biopsie), die auch tödlich verlaufen kann.
Blutung:
50 % der Patienten haben bis zu 7 Tage lang eine Hämaturie. Blutiges Sperma (Hämatospermie) in 30 %, dies kann bis zu einem Monat anhalten. Starke rektale Blutungen müssen tamponiert werden.
Weitere Komplikationen der Prostatabiopsie:
Harnverhalt (1–2 %), vasovagale Reaktion (5 %), Nebenwirkungen des Lokalanästhetikums wie Schwindel, Übelkeit, Synkope, Herzrhythmusstörungen und Krampfanfälle.
Prostatabiopsie in Augsburg
Sie wünschen moderne Prostatadiagnostik mit mpMRT und Fusionsbiopsie der Prostata in Augsburg beim Autor dieser Seite? Vereinbaren Sie einen Termin bei Dr. Manski in der Urologischen Gemeinschaftspraxis, Gögginger Str. 49 in Augsburg unter der Telefonnummer 0821 512200. Weitere Informationen zu Dr. Manski siehe Urologische Gemeinschaftspraxis Augsburg.
| Inguinale Lymphadenektomie | Suchen | TURP Resektion der Prostata |
Sachregistersuche: A B C D E F G H I J K L M N O P Q R S T U V W X Y Z
Literatur Prostatabiopsie
Arzneikommission der deutschen Ä rzteschaft, “Drug Safety Mail 2019-40: Information zu Fluorchinolonen: Prophylaktische Anwendung im Zuge urologischer Eingriffe,” 2019. [Online]. Available: https://www.akdae.de/Arzneimittelsicherheit/DSM/Archiv/2019-40.html.Hodge u.a. 1989 HODGE, K. K. ; MCNEAL, J. E. ; TERRIS, M. K. ; STAMEY, T. A.: Random systematic versus directed ultrasound guided transrectal core biopsies of the prostate.
In: J Urol
142 (1989), Nr. 1, S. 71–4; discussion 74–5
Lee, D. J.; Recabal, P.; Sjoberg, D. D.; Thong, A.; Lee, J. K.; Eastham, J. A.; Scardino, P. T.; Vargas, H. A.; Coleman, J. & Ehdaie, B. Comparative Effectiveness of Targeted Prostate Biopsy Using Magnetic Resonance Imaging Ultrasound Fusion Software and Visual Targeting: a Prospective Study.
The Journal of urology, 2016, 196, 697-702.
Loeb, S.; van den Heuvel, S.; Zhu, X.; Bangma, C. H.;
Schröder, F. H. & Roobol, M. J.
Infectious complications and
hospital admissions after prostate biopsy in a European randomized trial.
Eur. Urol. 2012,
61, 1110-1114.
Puech, P.; Rouvière, O.; Renard-Penna, R.;
Villers, A.; Devos, P.; Colombel, M.; Bitker, M.-O.; Leroy, X.;
Mège-Lechevallier, F.; Comperat, E.; Ouzzane, A. & Lemaitre, L.
Prostate
cancer diagnosis: multiparametric MR-targeted biopsy with cognitive and
transrectal US-MR fusion guidance versus systematic biopsy--prospective
multicenter study.
Radiology, 2013, 268, 461-469.
Rodriguez und Terris 1998 RODRIGUEZ, L. V. ;
TERRIS, M. K.:
Risks and complications of transrectal ultrasound guided prostate
needle biopsy: a prospective study and review of the literature.
In: J Urol
160 (1998), Nr. 6 Pt 1, S. 2115–20
Stamey 1995 STAMEY, T. A.:
Making the most out of six systematic sextant biopsies.
In: Urology
45 (1995), Nr. 1, S. 2–12
Wegelin, O.; Exterkate, L.; van der Leest, M.;
Kummer, J. A.; Vreuls, W.; de Bruin, P. C.; Bosch, J. L. H. R.; Barentsz,
J. O.; Somford, D. M. & van Melick, H. H. E.
The FUTURE Trial: A
Multicenter Randomised Controlled Trial on Target Biopsy Techniques Based
on Magnetic Resonance Imaging in the Diagnosis of Prostate Cancer in
Patients with Prior Negative Biopsies.
European urology, 2019,
75, 582-590.
Wysock, J. S.; Rosenkrantz, A. B.; Huang, W. C.;
Stifelman, M. D.; Lepor, H.; Deng, F.-M.; Melamed, J. & Taneja, S. S.
A
prospective, blinded comparison of magnetic resonance (MR)
imaging-ultrasound fusion and visual estimation in the performance of
MR-targeted prostate biopsy: the PROFUS trial.
European urology, 2014,
66, 343-351.
 English Version: Technique and complications of transrectal or transperineal Fusion Biopsy of the prostate
English Version: Technique and complications of transrectal or transperineal Fusion Biopsy of the prostate
Urologielehrbuch.de ohne Werbung
Diese Internetseite ermöglicht mit Hilfe von Werbung den Volltext-Zugriff auf das aktuelle Urologielehrbuch.de. Viele Bilder sind zum Schutz von Laien verpixelt oder ausgeblendet. Regelmäßig wiederkehrende (fachkundige) Leser können die Werbebanner abschalten und Zugriff auf alle Abbildungen erhalten: werden Sie Mitglied über die Crowdfunding-Plattform Steady und unterstützen Sie damit Urologielehrbuch.de.
Urologielehrbuch.de als Hardcover-Buch
 Aktuell, detailliert und übersichtlich: Urologielehrbuch.de wird auch als hochwertiges Hardcover-Buch veröffentlicht. Die 17. Auflage (Ausgabe 2024) ist seit Oktober 2024 verfügbar, siche Abschnitt Neuigkeiten für die Aktualisierungen und Links für den Buchkauf.
Aktuell, detailliert und übersichtlich: Urologielehrbuch.de wird auch als hochwertiges Hardcover-Buch veröffentlicht. Die 17. Auflage (Ausgabe 2024) ist seit Oktober 2024 verfügbar, siche Abschnitt Neuigkeiten für die Aktualisierungen und Links für den Buchkauf.